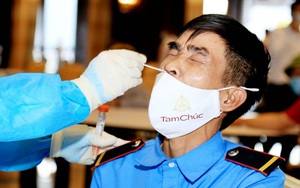
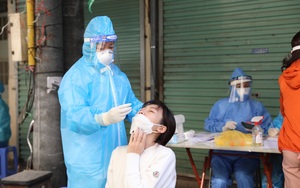
Vì sao Bộ KH&CN gỡ thông tin về bộ kit xét nghiệm liên quan Công ty Việt Á trên website?
Trước đó, ngày 26/4/2020 trên website của Bộ Khoa học và Công nghệ đã đăng tải nội dung thông tin có tiêu đề "Bộ KIT xét nghiệm Covid-19 của Việt Nam sản xuất vừa được Tổ chức Y tế thế giới chấp thuận" và ngay sau đó, một loạt các trang báo đã dẫn lại nội dung thông tin này.
Nội dung thông tin cho biết, bộ kit xét nghiệm Covid-19 LightPower iVA SARS-CoV-2 1st RT-rPCR KIT do Công ty Cổ phần Công nghệ Việt Á sản xuất đã được Tổ chức Y tế Thế giới (WHO) chấp thuận.
Sản phẩm được đánh giá theo Quy trình Danh sách Sử dụng Khẩn cấp (EUL) và cấp mã số EUL 0524-210-00.
Nội dung về bộ kit xét nghiệm của Công ty Việt Á từng được đăng tải trên website của Bộ KH&CN hiện đã không còn.
Cũng trong cuối tháng 4/2020, trong một cuộc họp báo do Bộ Khoa học - Công nghệ tổ chức, lãnh đạo Bộ này cũng đã khẳng định bộ kit xét nghiệm Covid-19 do Công ty Cổ phần Công nghệ Việt Á sản xuất đã được Tổ chức Y tế Thế giới (WHO) chấp thuận.
Tuy nhiên, theo bản cập nhật ngày 10/12/2021, sản phẩm này lại nằm trong danh sách mang tên "SARS‐CoV‐2 IVDs: sản phẩm không được chấp thuận cho EUL" đăng tải trên website chính thức của WHO, cũng với mã số EUL 0524-210-00.
Cụ thể, WHO cho biết bộ kit có tên LightPower iVASARS-CoV-2 1stRT-rPCR Kit của Công ty cổ phần Công nghệ Việt Á - địa chỉ tại phường 9, quận Phú Nhuận, TP.HCM, “không đủ điều kiện để vào chương trình mua sắm của WHO".
Theo WHO, tổ chức này trước đó đã yêu cầu Công ty cổ phần Công nghệ Việt Á cung cấp thông tin cập nhật về tình trạng hệ thống quản lý chất lượng của họ.
Tuy nhiên, các thông tin mà Công ty Việt Nam nộp lại được đánh giá không phải là bằng chứng đầy đủ cho thấy bộ sản phẩm của họ đáp ứng tiêu chuẩn ISO 13485: 2016 đối với thiết bị y tế.
Đặc biệt, đến chiều 20/12, nội dung đăng tải liên quan đến bộ kit xét nghiệm nói trên của Công ty Việt Á trên đã bị gỡ bỏ trên website - www.most.gov.vn của Bộ KH&CN.
Liên quan đến vấn đề này, chiều 20/12, PV Dân Việt đã liên hệ tới Bộ KH&CN, tuy nhiên phía cơ quan này chưa đưa ra câu trả lời chính thức nào.
Báo cáo công khai của WHO-EUL vào tháng 10/2020 về sản phẩm này có ghi rõ: "Kết quả: không được chấp thuận".
Tổ chức này giải thích thêm rằng sản phẩm "không đủ điều kiện tham gia đấu thầu của WHO". Theo đó, Công ty Cổ phần Công nghệ Việt Á được yêu cầu cung cấp thông tin cập nhật về tình trạng của hệ thống quản lý chất lượng của họ.
Sau khi xem xét tài liệu do Công ty Cổ phần Công nghệ Việt Á đệ trình nhằm hỗ trợ đánh giá bàn về hệ thống quản lý chất lượng của nhà sản xuất, thông tin nộp lên không phải là bằng chứng đầy đủ về việc tuân thủ ISO 13485: 2016 Trang thiết bị y tế - Hệ thống quản lý chất lượng - Yêu cầu đối với các mục đích quy định và các yêu cầu được mô tả trong "hướng dẫn về yêu cầu nộp: Chẩn đoán trong ống nghiệm (IVDS) Phát hiện axit nucleic SARS-COV-2, PQDX 347".