Xem lại bộ phim cũ, tôi đau đớn nhận ra mình đã bóp nghẹt con người thật của con suốt 18 năm
Tôi vừa đau đớn vừa cảm thấy mình thật thất bại.
 Tin tức
Tin tức
 Thế giới
Thế giới
 Nhà nông
Nhà nông
 Hội và Cuộc sống
Hội và Cuộc sống
 Đại đoàn kết dân tộc
Đại đoàn kết dân tộc
 Kinh tế
Kinh tế
 Thể thao
Thể thao
 Văn hóa - Giải trí
Văn hóa - Giải trí
 Xã hội
Xã hội
 Bạn đọc
Bạn đọc
 Nhà đất
Nhà đất
 Media
Media
 Chuyển động Sài Gòn
Chuyển động Sài Gòn
 Pháp luật
Pháp luật
 Dân Việt trò chuyện
Dân Việt trò chuyện
 Gia đình
Gia đình
 Đông Tây - Kim Cổ
Đông Tây - Kim Cổ
 Hà Nội hôm nay
Hà Nội hôm nay
 Radio Nông dân
Radio Nông dân
 Doanh nghiệp
Doanh nghiệp
Báo điện tử của Trung ương Hội Nông dân Việt Nam
Tổng biên tập: Nguyễn Văn Hoài
Phó Tổng Biên tập: Phan Huy Hà (Thường trực), Lưu Phan, Đỗ Thị
Sâm, Hoàng Sơn
Giấy phép hoạt động báo điện tử số 115/GP-BTTTT do Bộ TT-TT cấp ngày 01/3/2022 và giấy phép
sửa đổi, bổ sung số 55/GP-BVHTTDL do Bộ VHTTDL cấp ngày 11/6/2025
Bản quyền thuộc về Báo điện tử Dân Việt.
Mọi hình thức sao chép lại thông tin, hình ảnh phải được sự đồng ý bằng văn bản .
Vui lòng đăng nhập hoặc đăng ký để gửi bình luận
Xin chào, !
Bạn đã đăng nhập với email:
Đăng xuất
Quyết định 4361/QĐ-BYT ban hành ngày 10/9 về việc phê duyệt có điều kiện vắc xin cho nhu cầu cấp bách trong phòng, chống dịch bệnh Covid-19 cho vaccine Covid-19 Hayat-Vax.
Vaccine Covid-19 Hayat -Vax có thành phần hoạt chất, nồng độ/hàm lượng: Mỗi liều 0,5ml chứa 6.5 đơn vị kháng nguyên SARS-CoV-2 (tế bào vero) bất hoạt.
Dạng bào chế: Hỗn dịch tiêm với quy cách đóng gói là hộp 1 lọ chứa 1 liều 0,5ml và hộp 1 lọ chứa 2 liều; mỗi liều 0,5ml.
Sản phẩm do Beijing Institute of Biological Products Co., Ltd. - Trung Quốc sản xuất.
Cơ sở đóng gói sơ cấp, thứ cấp và xuất xưởng: Julphar (Gulf Pharmaceutical Industries) - Các tiểu Vương quốc Ả rập thống nhất.
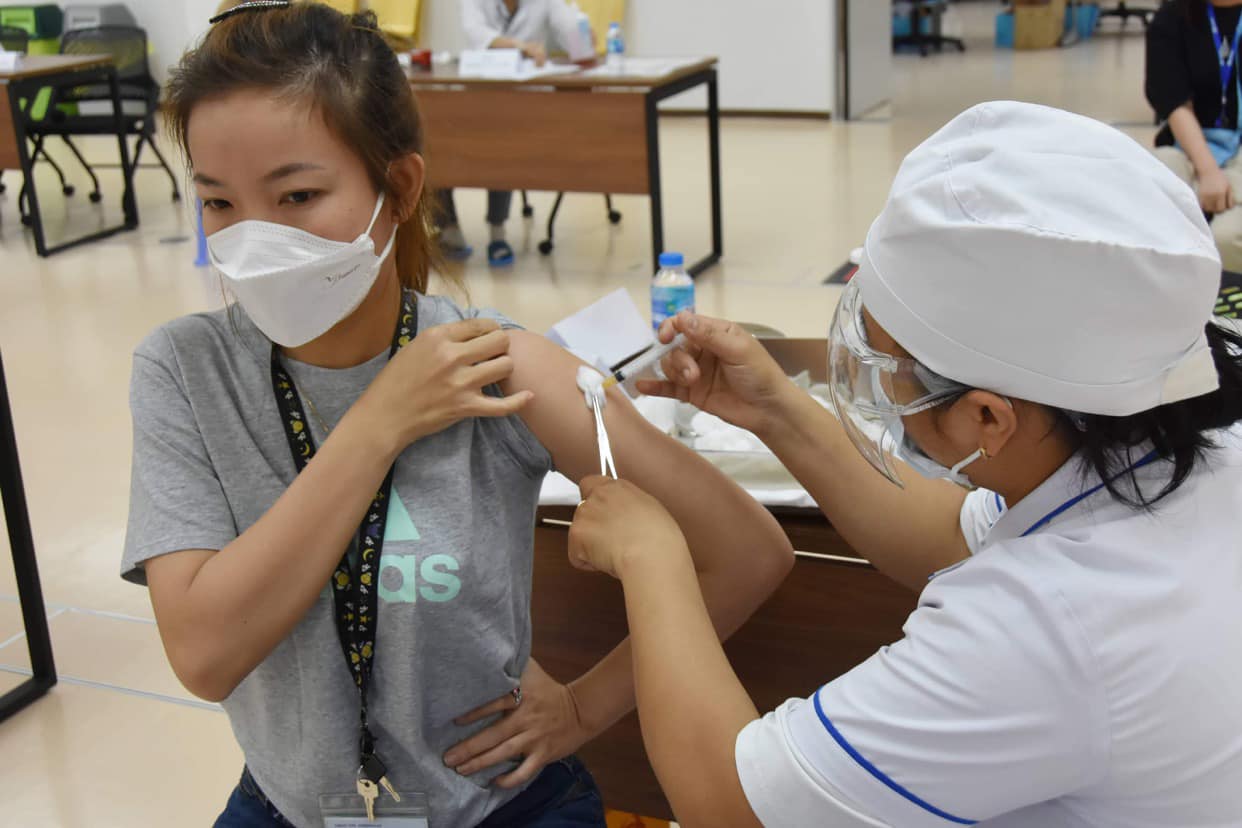
Tiêm vaccine Covid-19 tại TP.HCM. Ảnh BYT
Cơ sở đề nghị phê duyệt vaccine Covid-19 Hayat-Vax là Công ty Cổ phần Y dược phẩm Vimedimex.
Các điều kiện đi kèm việc phê duyệt vaccine Hayat -Vax cho nhu cầu cấp bách trong phòng, chống dịch bệnh Covid-19 được ban hành tại Phụ lục kèm theo Quyết định 4361/QĐ-BYT.
Theo Quyết định, Cục Quản lý Dược có trách nhiệm: Cấp phép nhập khẩu vaccine Hayat -Vax theo quy định tại Điều 67 Nghị định 54/2017/NĐ-CP khi nhận được hồ sơ của cơ sở nhập khẩu. Đồng thời thực hiện đúng quy định của pháp luật về quản lý nhập khẩu, quản lý chất lượng vắc xin nhập khẩu.
Cục Khoa học công nghệ và Đào tạo có trách nhiệm: Lựa chọn đơn vị có đủ điều kiện đánh giá tính an toàn, hiệu quả của vắc xin trên cơ sở ý kiến tư vấn của Hội đồng tư vấn sử dụng vaccine, sinh phẩm y tế của Bộ Y tế trong quá trình sử dụng;
Đồng thời hướng dẫn, chỉ đạo đơn vị có đủ điều kiện quy định tổ chức thực hiện việc đánh giá tính an toàn, hiệu quả của vaccine Hayat -Vax trên cơ sở ý kiến tư vấn của Hội đồng tư vấn sử dụng vaccine, sinh phẩm y tế của Bộ Y tế trong quá trình sử dụng.
Cục Y tế Dự phòng thực hiện các trách nhiệm liên quan đến tiêm chủng vaccine Hayat -Vax được quy định tại Quyết định số 1464/QĐ-BYT ngày 05/03/2021 của Bộ trưởng Bộ Y tế về việc ban hành hướng dẫn tiếp nhận, bảo quản, phân phối và sử dụng vaccine Covid-19; Quyết định số 3355/QĐ-BYT ngày 8/7/2021 của Bộ trưởng Bộ Y tế về việc phê duyệt kế hoạch triển khai chiến dịch tiêm vaccine Covid-19 năm 2021- 2022 và Công văn số 5800/VPCP-KGVX ngày 20/8/2021 của Văn phòng Chính phủ về việc Công ty Cổ phần Y dược phẩm Vimedimex đề nghị cấp phép khẩn cấp vaccine Hayat -Vax.
Viện Kiểm định Quốc gia vaccine và sinh phẩm y tế có trách nhiệm tiến hành kiểm định và cấp Giấy chứng nhận xuất xưởng lô vaccine Hayat -Vax trước khi đưa ra sử dụng.
Tôi vừa đau đớn vừa cảm thấy mình thật thất bại.
Tháng Giêng năm Gia Khánh thứ 4, Thái thượng Hoàng Càn Long Đế qua đời, Vương Hoài Tổ dâng tấu vạch tội Hòa Thân. Gia Khánh Đế lập tức ra chiếu lệnh cách chức Hòa Thân, giam vào ngục, xử tử hình.
Theo lịch sử, Tần Mục công là người đã đưa nước Tần từ vị trí một chư hầu xa xôi hẻo lánh ở phía Tây bắc Trung Quốc vươn lên địa vị bá chủ thời Xuân Thu. Và tất nhiên, thành công này không thể không nhắc tới “quân sư” đại tài Bách Lý Hề.
NATO khẳng định khối lượng vũ khí viện trợ cho Ukraine không hề suy giảm, bất chấp những thay đổi trong chính sách của Mỹ sau khi ông Donald Trump trở lại cầm quyền, theo UATV English.
HLV Đoàn Minh Hải hiện đang được coi là một trong những ứng cử viên sáng giá có thể dẫn dắt ĐT nữ Việt Nam khi HLV Mai Đức Chung nhiều khả năng rời "ghế nóng".
Á khôi 2 Hoa khôi Duyên dáng Áo dài Việt Nam 2025 Đinh Thị Phương Anh sở hữu nhan sắc ngọt ngào, duyên dáng
Ngày 23/12, tại trụ sở UBND xã Mường É, tỉnh Sơn La, Báo Nông thôn Ngày nay/Điện tử Dân Việt phối hợp với Công ty Ty DVL Ventures – Hà Vy và các nhà hảo tâm tổ chức chương trình “Chợ yêu thương vùng cao Mường É”. Tham dự chương trình có lãnh đạo xã Mường É, đại diện các trường học trên địa bàn cùng đông đảo bà con các dân tộc trong xã.
Ngày 11/12/2025 tại Hà Tĩnh - Ngân hàng TMCP Đông Nam Á (SeABank, HOSE:SSB) đã trao tặng 670.984 cây keo giống cho các hộ dân tại xã Kỳ Hoa, tỉnh Hà Tĩnh nhằm phục hồi hệ sinh thái rừng bị tàn phá nghiêm trọng bởi cơn bão Bualoi, đồng thời tạo sinh kế bền vững cho người dân địa phương. Qua đó nâng tổng số cây Ngân hàng trao tặng và trồng vượt 1 triệu cây xanh trên khắp cả nước nhằm phủ xanh đất trống, đồi núi trọc.
Mùa lễ hội cuối năm mang đến không khí rộn ràng của mua sắm, gặp gỡ và những chuyến đi nối tiếp nhau. Đây cũng là lúc những người tiêu dùng thông thái lên kế hoạch để chi tiêu hợp lý và “tận dụng” tối đa các ưu đãi từ các ngân hàng hay các thương hiệu, cho trải nghiệm mua sắm trong giai đoạn cao điểm thêm trọn vẹn.
Theo các nguồn tin, mâu thuẫn giữa Ngoại trưởng Mỹ Marco Rubio và Đặc phái viên Steve Witkoff đang ngày càng sâu sắc, khi hai bên bất đồng gay gắt về cách thức chấm dứt cuộc chiến tại Ukraine, theo Intellinews.
Lãnh đạo LĐBĐ Malaysia xác nhận "đầu hàng" trước FIFA; HLV Thawatchai quyết “sửa sai” ở giải U23 châu Á; Ronaldo lọt Top 5 cầu thủ có thể gây thất vọng ở World Cup 2026; Disasi sắp chia tay Chelsea; Bruno Fernandes đi ăn tối cùng gia đình.
SEA Games 33 đã chính thức khép lại, đánh dấu một kỳ đại hội nhiều cảm xúc và dấu ấn đáng nhớ của thể thao Việt Nam. Những tài năng thể thao đang được Quỹ Phát triển Tài năng Việt tài trợ học bổng Đại học đã thi đấu đầy nỗ lực và giành được những tấm huy chương giá trị.
“Khu vực kinh tế tư nhân không chỉ dừng ở mong muốn tham gia, mà đã bắt đầu chuyển động thực chất, tìm kiếm đối tác, chuẩn bị nguồn lực để bước vào đảm nhận những dự án mang tầm quốc gia”, TS Nguyễn Minh Phong nhận định.
Nhiều ngôi sao hàng đầu trong showbiz Việt bị bắt giam trong năm qua như Nguyễn Thúc Thùy Tiên, Trương Ngọc Ánh, Công Trí...
Sư thầy chủ trì hôn lễ đã hé lộ hành động xúc động khi Shin Min Ah từng đội gạo lên núi cầu nguyện cho Kim Woo Bin vượt qua bạo bệnh khiến quan khách rơi nước mắt.
Bệnh nhân nhập viện trong tình trạng đau đầu, chóng mặt, yếu tứ chi, tăng phản xạ gân xương và phân ly cảm giác, không tự sinh hoạt được, ăn qua sonde dạ dày.
Với việc chơi xuất sắc tại SEA Games 33, góp công lớn giúp U22 Việt Nam giành HCV, tiền đạo Nguyễn Đình Bắc đã vinh dự nhận được bằng khen từ Bộ trưởng Bộ Công an.
Tại kỳ họp thứ 35, HĐND tỉnh Hưng Yên đã thực hiện quy trình cho thôi làm nhiệm vụ đại biểu HĐND tỉnh khóa XVII, nhiệm kỳ 2021 - 2026 đối với ông Nguyễn Quốc Vương - nguyên Phó Giám đốc Công an tỉnh do được điều động, phân công công tác khác.
Theo tử vi ngày mai, 4 con giáp dũng cảm tiến về phía trước, tài lộc liên tục đổ về, có cơ hội thoát nghèo trở nên giàu có vào dịp Giáng sinh.
Tỉnh Đồng Tháp mới (sau sáp nhập tỉnh Tiền Giang) tập trung tháo gỡ vướng mắc, tăng tốc giải ngân 100% vốn đầu tư công năm 2025, thúc đẩy tăng trưởng GRDP trên 8%.
Thất bại của châu Âu trong việc sử dụng tài sản Nga bị phong tỏa để tài trợ cho Ukraine không chỉ phơi bày sự chia rẽ nội khối, mà còn đẩy Kiev vào thế ngày càng khó trụ vững trong cuộc chiến tiêu hao với Moscow, theo Politico.
Về nhà sau khi cùng U22 Việt Nam giành HCV môn bóng đá nam SEA Games 33, trung vệ Phạm Lý Đức đã giao lưu bóng đá và phát quà từ thiện cho bà con tại quê nhà Long Thuận, Tây Ninh.
Bệnh nhân nhập viện trong tình trạng co giật, đau đầu, không hề nghĩ rằng mình bị nhiễm ký sinh trùng nguy hiểm.
Triệu Lộ Tư vực dậy sự nghiệp rực rỡ nhờ tác phẩm thành công vang dội trong khi Ngu Thư Hân đối mặt với làn sóng tẩy chay mạnh mẽ vì hàng loạt bê bối đời tư cùng dự án phim thua lỗ nặng nề.
Chính phủ quần đảo Marshall bắt đầu giải ngân khoản trợ cấp 200 USD mỗi quý cho mọi công dân cư trú trên lãnh thổ nhằm giảm bớt áp lực tài chính và ngăn chặn làn sóng di cư.
Không khí Giáng sinh 2025 đang "bùng nổ" tại khu vực Nhà thờ Lớn. Toạ độ "sống ảo" này đang thu hút hàng ngàn lượt khách đổ về chụp ảnh, check-in.
Công an TP Đà Nẵng cho biết đang khẩn trương truy bắt nghi phạm dùng hung khí tấn công một người phụ nữ trên địa bàn phường An Khê, hiện đối tượng vẫn đang bỏ trốn.
Trung ương biểu quyết thông qua với số phiếu tập trung cao nhân sự giới thiệu tham gia Ban Chấp hành Trung ương Đảng khóa XIV; giới thiệu nhân sự tham gia Bộ Chính trị, Ban Bí thư, lãnh đạo chủ chốt của Đảng và Nhà nước khóa XIV, nhiệm kỳ 2026 - 2031, để trình Đại hội Đại biểu toàn quốc lần thứ XIV của Đảng.
Với kinh nghiệm 30 năm trồng sầu riêng, ông Nguyễn Hoàng Anh ở ấp 4, xã Đại Hải, TP Cần Thơ giờ có thu nhập hàng tỷ đồng mỗi năm. Khi thị trường ngày càng có nhu cầu cao về sản phẩm sầu riêng sạch, ông Hoàng Anh nhanh chóng chuyển hướng trồng sầu riêng hữu cơ...
Sau khi gia nhập Mạng lưới Thành phố học tập toàn cầu của UNESCO, TP.HCM lên kế hoạch số hóa dữ liệu học tập cá nhân và đẩy mạnh phân cấp cho cơ sở sau khi sắp xếp đơn vị hành chính.
