- Bầu cử Tổng thống Mỹ 2024
- Nhìn lại Hội nghị Thủ tướng đối thoại với nông dân 2023
- Chủ tịch Hội NDVN- Bộ trưởng TNMT lắng nghe nông dân nói
- Kỷ nguyên mới - Kỷ nguyên vươn mình
- Tháo gỡ điểm nghẽn thể chế
- Kỳ họp thứ 8 Quốc hội khóa XV
- Căng thẳng Triều Tiên - Hàn Quốc đang gia tăng
- Diễn đàn Nông dân quốc gia lần thứ IX - 2024
Chủ đề nóng
- Đăng nhập
- Đăng ký
- ×
Vui lòng đăng nhập hoặc đăng ký để gửi bình luận
Khi nhấn đăng nhập đồng nghĩa với việc bạn đã đồng ý với điều khoản sử dụng của báo Dân Việt
Đăng nhập
Họ và tên
Mật khẩu
Mã xác nhận

Khi nhấn đăng ký đồng nghĩa với việc bạn đã đồng ý với
điều khoản sử dụng của
báo Dân Việt
Đăng ký
Xin chào, !
Bạn đã đăng nhập với email:
Đăng xuất
Bộ Y tế nói gì về đề xuất Thủ tướng cấp phép khẩn cho vắc xin Covid của Nanogen?
Diệu Linh
Thứ tư, ngày 23/06/2021 06:51 AM (GMT+7)
Đại diện Bộ Y tế cho biết, để quyết định có cấp phép khẩn cấp vắc xin Covid-19 hay không, Bộ Y tế cần có các dữ liệu khoa học.
Bình luận
0
Về việc Công ty cổ phần công nghệ sinh học dược Nanogen (Công ty Nanogen) đề xuất Thủ tướng cấp phép khẩn cấp cho vắc xin Covid-19 Nano Covax, tối 22/6, TS Nguyễn Ngô Quang - Phó cục trưởng Cục Khoa học công nghệ và đào tạo (Bộ Y tế) - khẳng định: "Kiến nghị là quyền của doanh nghiệp, còn việc cho phép hay không thuộc thẩm quyền của các cơ quan chuyên môn, căn cứ theo các quy định.
Việc ra quyết định cấp phép khẩn cấp một loại vắc xin phụ thuộc vào rất nhiều yếu tố. Để quyết định có cấp phép khẩn cấp hay không, Bộ Y tế cần có các dữ liệu khoa học".
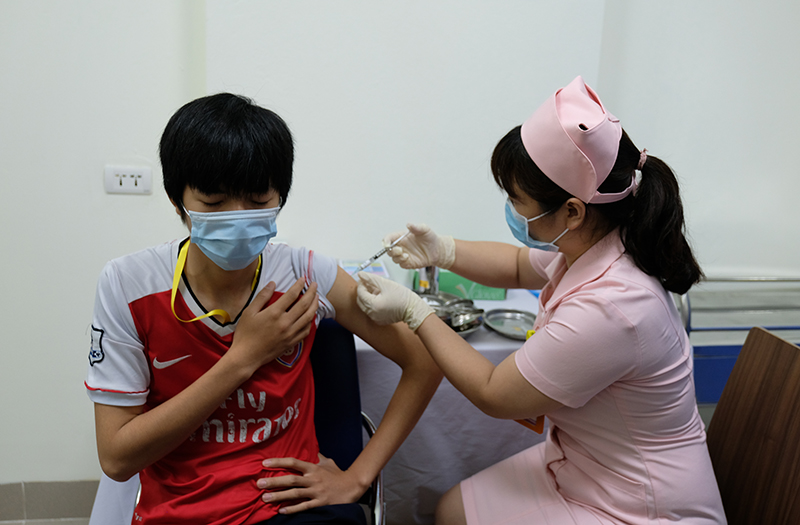
Tình nguyện viên được tiêm vắc xin Covid-19 Nano Covax. Ảnh Trần Minh
Theo ông Quang, việc cấp phép vắc xin phải trả lời được 3 câu hỏi lớn. Đó là: Có an toàn không? Có sinh miễn dịch không? Và điều đặc biệt quan trọng đó là có hiệu lực bảo vệ không? Cho dù trong bối cảnh dịch Covid-19 cấp bách như hiện nay cũng vẫn phải dựa trên nguyên tắc đầy đủ các dữ liệu khoa học, trả lời được 3 câu hỏi trên.
Ông Quang nhận định, vắc xin Covid-19 Nano Covax do Công ty Nanogen sản xuất mới đang thử nghiệm giai đoạn 3a. Cụ thể là mới thử nghiệm trên 1000 người. Đây là số lượng nhỏ chưa mang tính cộng đồng so với hàng trăm triệu người sử dụng vắc xin sau này.
Đề cương thử nghiệm giai đoạn 3 mà Bộ Y tế phê duyệt (ngày 11/6) cần thử nghiệm trên 13.000 người. Đồng thời cũng cần có thời gian để đánh giá tính sinh miễn dịch và hiệu lực bảo vệ của vắc xin. Để có đủ căn cứ khoa học đánh giá cần phải theo dõi sau tiêm mũi 1 sau 36 ngày, 45 ngày và 56 ngày.
"1.000 người chưa nói lên điều gì nhiều", ông Quang nói.
Theo ông Quang, quan điểm của Bộ Y tế cũng như cá nhân ông là hoàn toàn ủng hộ cho sự nghiên cứu phát triển vắc xin Covid-1 trong nước để chủ động được nguồn vắc xin của Việt Nam. Tuy nhiên, để có 1 vắc xin tiêm rộng rãi cho người dân, về nguyên tắc Bộ Y tế phải có các dữ liệu về an toàn, tính sinh miễn dịch và đặc biệt là hiệu lực bảo vệ. Mục tiêu của ngành y tế là bảo vệ sức khỏe người dân nên phải hết sức cân nhắc giữa lợi ích và nguy cơ.
"Việc phê duyệt cấp phép thận trọng không phải làm khó doanh nghiệp", ông Quang khẳng định.
Ông Quang cũng đánh giá hiện nay các dữ liệu thử nghiệm giai đoạn 1 và 2 của vắc xin Covid-19 Nano Covax là an toàn, có tính sinh miễn dịch nhưng hiệu lực bảo vệ như nào vẫn đang trong thời gian nghiên cứu, thử nghiệm tiếp.
Trước đó, ngày 22/6, ông Hồ Nhân, Tổng Giám đốc Công ty Nanogen cho biết, Công ty đã gửi kiến nghị Chính phủ để vắc xin Nano Covax sớm được cấp phép khẩn cấp có điểu kiện, tượng tự như các loại vắc xin của Nga, Trung Quốc và Ấn Độ.

Các mẫu vắc xin Covid-19 của Nanogen. Ảnh D.L
Trong ngày 22/6, PGS.TS Chử Văn Mến, Giám đốc Trung tâm Thử nghiệm lâm sàng và tương đương sinh học, Học viện Quân y, Bộ Quốc phòng cho biết. đã có 1000 người được thử nghiệm vắc xin Covid-19 Nano Covax giai đoạn 3, liều 25mcg (liều duy nhất). Hiện tại sức khỏe của các tình nguyện viên đều ổn định.
Theo đề cương thử nghiệm lâm sàng giai đoạn 3 vắc xin Covid-19 Nano Covax, việc thử nghiệm được thực hiện tại nhiều trung tâm trong nước trên 13.000 người thử nghiệm; chỉ thực hiện tiêm nhóm liều duy nhất 25 mcg và nhóm tiêm giả dược đối chứng.
Giai đoạn 3 không chỉ đánh giá tính an toàn, sinh miễn dịch, giai đoạn 3 thử nghiệm vắc xin Nano Covax nhằm mục đích đánh giá yếu tố hiệu lực bảo vệ của vắc xin đối với cộng đồng - đây là yếu tố hai giai đoạn trước chưa được thực hiện.
Qua 2 giai đoạn đầu, kết quả thử nghiệm cho thấy, 100% tình nguyện viên đều sinh miễn dịch tốt. Tỷ lệ chuyển đổi huyết thanh đạt trên 99%.
Tin cùng sự kiện: Bùng phát đợt dịch Covid-19 thứ 4
- "Thích ứng an toàn, linh hoạt, kiểm soát hiệu quả dịch Covid-19" là thế nào?
- Diễn biến dịch Covid-19: Hà Nội đột ngột tăng mạnh số ca nhiễm mới
- Hà Nội: Cận cảnh phun khử khuẩn các ngõ xóm tại phường Phú Đô sau khi nâng cấp độ dịch
- Tình hình Covid-19 ngày 14/11: Còn hơn 140.000 ca đang được theo dõi và điều trị
Mời các bạn đồng hành cùng báo Dân Việt trên mạng xã hội Facebook để nhanh chóng cập nhật những tin tức mới và chính xác nhất.
Tin cùng chuyên mục
Xem theo ngày
Xem
Tin nổi bật









Vui lòng nhập nội dung bình luận.