- Bầu cử Tổng thống Mỹ 2024
- Nhìn lại Hội nghị Thủ tướng đối thoại với nông dân 2023
- Chủ tịch Hội NDVN- Bộ trưởng TNMT lắng nghe nông dân nói
- Kỷ nguyên mới - Kỷ nguyên vươn mình
- Tháo gỡ điểm nghẽn thể chế
- Kỳ họp thứ 8 Quốc hội khóa XV
- Căng thẳng Triều Tiên - Hàn Quốc đang gia tăng
- Diễn đàn Nông dân quốc gia lần thứ IX - 2024
Chủ đề nóng
- Đăng nhập
- Đăng ký
- ×
Vui lòng đăng nhập hoặc đăng ký để gửi bình luận
Khi nhấn đăng nhập đồng nghĩa với việc bạn đã đồng ý với điều khoản sử dụng của báo Dân Việt
Đăng nhập
Họ và tên
Mật khẩu
Mã xác nhận

Khi nhấn đăng ký đồng nghĩa với việc bạn đã đồng ý với
điều khoản sử dụng của
báo Dân Việt
Đăng ký
Xin chào, !
Bạn đã đăng nhập với email:
Đăng xuất
Bao nhiêu chuyên gia, nhà khoa học kiến nghị Bộ Y tế cấp phép cho kit test của Công ty Việt Á?
PVCT
Thứ ba, ngày 04/01/2022 15:26 PM (GMT+7)
Trong báo cáo của Chính phủ gửi Quốc hội, các vấn đề có liên quan đến vụ việc xảy ra tại Công ty cổ phần Công nghệ Việt Á (Công ty Việt Á) đã được thông tin cụ thể.
Bình luận
0
Theo báo cáo của Chính phủ gửi Quốc hội, tại thời điểm đầu năm 2020, chưa có sinh phẩm chẩn đoán SARS-CoV-2 nào (kể cả nhập khẩu) được cấp phép lưu hành tại Việt Nam. Trên thế giới cũng có ít sản phẩm được đăng ký lưu hành. Tổ chức Y tế thế giới (WHO) công nhận sinh phẩm đầu tiên vào ngày 7/4/2020), các nước thường sử dụng các sản phẩm được phát triển, sản xuất bởi các phòng thí nghiệm.

Chủ tịch HĐQT, Tổng Giám đốc Công ty Việt Á Phan Quốc Việt đã bị khởi tố, bắt tạm giam. Ảnh Bộ Công an
Tại Việt Nam, số lượng sinh phẩm hoàn toàn do WHO, Trung tâm Kiểm soát và phòng ngừa bệnh tật Hoa Kỳ (USCDC) tài trợ và luôn trong tình trạng khan hiếm, bị động, chờ đợi. Tình trạng đó tạo áp lực rất lớn cho công tác phòng chống dịch.
Trong bối cảnh đó, Bộ Khoa học và Công nghệ đã phối họp với các đơn vị triển khai nhiệm vụ khoa học công nghệ cấp quốc gia, trong đó có nhiệm vụ nghiên cứu chế tạo bộ sinh phẩm RT-PCR và Realtime -PCR phát hiện chủng vi rút corona mới 2019 (2019-nCoV) do Học viện Quân y là đơn vị chủ trì và Công ty Việt Á để phối hợp thực hiện.
Đề tài này đã được Hội đồng đánh giá nghiệm thu giai đoạn 1 do Bộ Khoa học và Công nghệ thành lập họp ngày 3/3/2020, toàn bộ 8/8 chuyên gia và nhà khoa học là thành viên Hội đồng nhất trí kiến nghị Bộ Y tế xem xét cấp phép sử dụng.
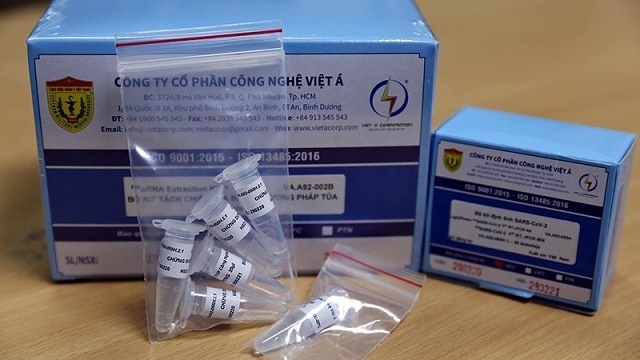
Kit xét nghiệm của Công ty Việt Á. Ảnh: Bộ KH-CN
Sau khi nhận được hồ sơ đăng ký cấp số lưu hành của Công ty Việt Á về việc cấp phép sử dụng test kit phát hiện chủng mới của vi rút Corona (SARS-CoV-2) trong điều kiện phòng, chống dịch khẩn cấp, Bộ Y tế đã có văn bản hướng dẫn công ty này nộp bổ sung hồ sơ đăng ký.
Căn cứ kiến nghị của Hội đồng đánh giá, nghiệm thu của Bộ Khoa học và Công nghệ nêu trên, kết quả kiểm định độc lập của Viện Vệ sinh dịch tễ Trung ương, Hội đồng tư vấn cấp số lưu hành sinh phẩm chẩn đoán in vitro sử dụng trong phòng xét nghiệm của Bộ Y tế đã họp xem xét và thống nhất đề nghị cấp phép lưu hành tạm thời trong thời gian 6 tháng phục vụ xét nghiệm sàng lọc để đáp ứng yêu cầu cấp bách trong phòng, chống dịch và trong thời gian này phải tiếp tục đánh giá chất lượng.
Theo báo cáo của Học viện Quân y, bộ kit được sản xuất tại cơ sở có hệ thống quản lý được chứng nhận phù hợp tiêu chuẩn ISO 13485:2016. Các tiêu chuẩn của bộ kit đã được kiểm định độc lập tại Viện Vệ sinh Dịch tễ Trung ương, Bộ Y tế. Kết quả kiểm định sau khi sử dụng 5 loại thiết bị phổ biến ở các cơ sở y tế đều cho kết quả chính xác 100% tại tất cả các thiết bị và tất cả các lần thử nghiệm.
Sau khi được cấp phép tạm thời, Công ty Việt Á tiếp tục nộp hồ sơ đề nghị được đăng ký lưu hành chính thức. Căn cứ ý kiến của 3 nhóm chuyên gia thẩm định hồ sơ về pháp lý, hồ sơ về chất lượng và hồ sơ về hiệu quả chẩn đoán, Bộ Y tế đã yêu cầu và Công ty Việt Á đã bổ sung hồ sơ.
Trên cơ sở đó, Hội đồng tư vấn đã họp đánh giá và kiến nghị Bộ Y tế cấp phép đăng ký lưu hành của Công ty Việt Á và Công ty Sao Thái Dương, có giá trị 5 năm. Theo báo cáo của Học viện Quân y là đơn vị tổ chức chủ trì nhiệm vụ sẽ tiếp tục có các đánh giá đến tháng 10/2021.
Với vụ việc vi phạm của Công ty Việt Á, Chính phủ đánh là "vụ việc vi phạm pháp luật nghiêm trọng" đã được Chính phủ, Thủ tướng Chính phủ chỉ đạo Bộ Công an tiến hành điều tra và khởi tố các cá nhân vi phạm.
Báo cáo chỉ rõ: Công ty Việt Á đã lợi dụng tình trạng dịch bệnh để trục lợi, đồng thời một số cá nhân đã vi phạm các quy định trong tổ chức thực hiện mua sắm, đấu thầu và dụng chức vụ, quyền hạn trong khi thi hành công vụ.
Vụ án đã được Ban Chỉ đạo Trung ương phòng, chống tham nhũng, tiêu cực đưa vào diện Ban Chỉ đạo theo dõi. Thủ tướng Chính phủ đã có các văn bản chỉ đạo khẩn trương tiến hành điều tra và xử lý nghiêm các trường hợp vi phạm pháp luật, lợi dụng dịch bệnh để trục lợi bất chính.
Tin cùng chủ đề: Công ty Việt Á nâng khống giá kit test Covid-19
- Công an làm việc với Giám đốc CDC Đắk Lắk về việc mua kit test của Công ty Việt Á
- Vụ Giám đốc CDC Bình Phước “nhận quà” của Công ty Việt Á: Cán bộ Sở Y tế làm việc với Bộ Công an
- Đại biểu Quốc hội: Việt Á chi “hoa hồng” gần 800 tỷ đồng, thật khủng khiếp nhưng số tiền có thể lớn hơn
- Bình Dương lên tiếng về việc mua 6 máy xét nghiệm PCR giá hơn 23 tỷ đồng của Công ty Việt Á
Mời các bạn đồng hành cùng báo Dân Việt trên mạng xã hội Facebook để nhanh chóng cập nhật những tin tức mới và chính xác nhất.
Tin cùng chuyên mục
Xem theo ngày
Xem
Tin nổi bật










Vui lòng nhập nội dung bình luận.