- Bầu cử Tổng thống Mỹ 2024
- Nhìn lại Hội nghị Thủ tướng đối thoại với nông dân 2023
- Chủ tịch Hội NDVN- Bộ trưởng TNMT lắng nghe nông dân nói
- Kỷ nguyên mới - Kỷ nguyên vươn mình
- Tháo gỡ điểm nghẽn thể chế
- Kỳ họp thứ 8 Quốc hội khóa XV
- Căng thẳng Triều Tiên - Hàn Quốc đang gia tăng
- Diễn đàn Nông dân quốc gia lần thứ IX - 2024
Chủ đề nóng
- Đăng nhập
- Đăng ký
- ×
Vui lòng đăng nhập hoặc đăng ký để gửi bình luận
Khi nhấn đăng nhập đồng nghĩa với việc bạn đã đồng ý với điều khoản sử dụng của báo Dân Việt
Đăng nhập
Họ và tên
Mật khẩu
Mã xác nhận

Khi nhấn đăng ký đồng nghĩa với việc bạn đã đồng ý với
điều khoản sử dụng của
báo Dân Việt
Đăng ký
Xin chào, !
Bạn đã đăng nhập với email:
Đăng xuất
Lên kế hoạch test nhanh SARS-CoV-2 khi mở cửa trở lại các đường bay quốc tế
An Vũ
Thứ tư, ngày 09/09/2020 12:27 PM (GMT+7)
Bộ Khoa học và Công nghệ mới đây đã có buổi làm việc cùng đại diện Bộ Y tế, các đơn vị sản xuất kit xét nghiệm SARS-CoV-2, viện nghiên cứu... để bàn các phương án đảm bảo việc sử dụng sinh phẩm kiểm tra nhanh.
Bình luận
0
Chưa có quyết định cuối cùng của Chính phủ nhưng chủ trương nối lại đường bay thương mại đã được bàn thảo trong các cuộc họp gần đây, trong đó điều kiện tiên quyết là thay đổi chiến lược xét nghiệm, với nội dung trọng tâm là tập trung xét nghiệm nhanh tại các sân bay, đảm bảo vừa nhanh vừa chính xác.
Tại buổi làm việc, Thứ trưởng Bộ Khoa học và Công nghệ Phạm Công Tạc đề nghị các nhà khoa học và chuyên gia đề xuất các phương án xét nghiệm, đảm bảo việc không bỏ sót nguồn nhiễm SARS-CoV-2 lây ra cộng đồng khi Việt Nam mở cửa các đường bay quốc tế sắp tới.
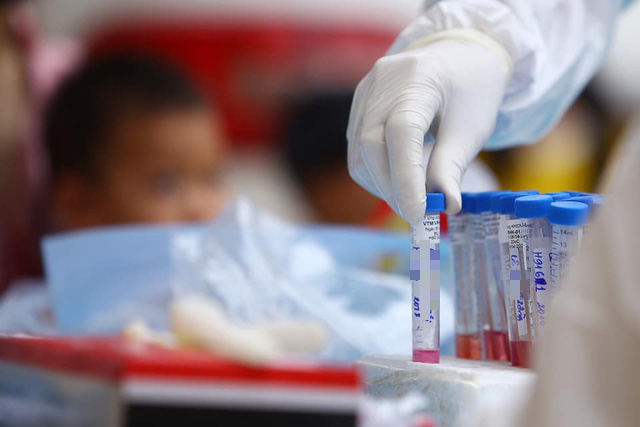
Việt Nam lên phương án test nhanh SARS-CoV-2 khi mở cửa đường bay quốc tế.
Theo báo cáo của Bộ Y tế, đến nay FDA Hoa Kỳ đã phê duyệt danh mục gồm 176 sinh phẩm phát hiện SARS-CoV-2, bao gồm 130 sinh phẩm RT-PCR; 40 sinh phẩm miễn dịch (phát hiện kháng thể); 1 sinh phẩm RT-LAMP; 4 sinh phẩm nhanh kháng nguyên và 1 sinh phẩm giải trình tự gene.
Hiện tại, Việt Nam có 4 loại sinh phẩm, gồm 2 loại kit sử dụng kỹ thuật phát hiện kháng thể kháng SARS-CoV-2 trong máu của bệnh nhân COVID-19 và 2 loại dùng kỹ thuật công nghệ sinh học (RT-PCR) và RT-LAMP để phát hiện virus SARS-CoV-2. Trong số này có 3 loại được Bộ Y tế cấp phép sử dụng.
Theo đó, khi Việt Nam mở lại các đường bay quốc tế, yêu cầu đặt ra lớn nhất là phải đảm bảo xét nghiệm nhanh. Về yếu tố này, kit phát hiện nhanh kháng nguyên và kháng thể SARS-CoV-2 có thể đảm bảo. Nhược điểm là không chính xác và không có ý nghĩa chẩn đoán.
Ở phương pháp này phù hợp đối với những trường hợp nhiễm SARS-CoV-2 nhưng không có triệu chứng. Tuy nhiên, sau đó vẫn cần phải xét nghiệm lại bằng RT-PCR mới khẳng định chính xác trường hợp âm hay dương tính với SARS-CoV-2.
Theo ông Vũ Đình Hiệp, Đại diện Công ty cổ phần Công nghệ Việt Á, đơn vị đang phối hợp cùng Học Viện Quân y sản xuất kit RT-PCR cho rằng, trong trường hợp tìm kiếm các ca nhiễm sót ngoài cộng đồng, test nhanh (kháng nguyên, kháng thể) sẽ phát huy tác dụng. Nhưng để đảm bảo không "lọt lưới" thì phương pháp real-time PCR tin cậy hơn.
Ông Hiệp cũng đề nghị trước mắt có thể đặt phòng Lab ngay tại ba sân bay lớn gồm Hà Nội, TP.HCM và Đà Nẵng và cửa khẩu. Hiện nay nhiều bệnh viện dã chiến đã có Lab và có thể sử dụng phương pháp trộn mẫu. Theo tính toán, giá xét nghiệm một mẫu là 20 USD (test nhanh là 17,5 USD một mẫu).
GS.TS Lê Bách Quang, Chương trình Khoa học công nghệ trọng điểm cấp nhà nước cho rằng, việc quyết định sử dụng phương pháp nào thuộc về các nhà quản lý. Tuy nhiên ông mong muốn các đơn vị sản xuất trong nước cùng ngồi lại với nhau để xây dựng một sản phẩm mang tầm quốc gia đảm bảo đủ ba yếu tố (nhanh, rẻ, chính xác) chứ không riêng doanh nghiệp nào.
Đại diện Cục Y tế dự phòng Cục Khoa học công nghệ và Đào Tạo (Bộ Y tế) thì mong muốn các nhà khoa học, đơn vị sản xuất cùng tính toán lại để tạo ra kit thử tăng độ nhạy, độ đặc hiệu, đảm bảo sàng lọc không bỏ sót ca bệnh.
Bộ Y tế cũng xây dựng quy trình chuẩn trong tình hình mới trình Chính phủ, đảm bảo thực hiện các xét nghiệm nhanh, phát hiện sớm các ca nhiễm, nghi nhiễm, tránh lây lan cộng đồng.
Hồi tháng 4/2020, Tổ chức Y tế thế giới (WHO) đã công nhận bộ kít xét nghiệm Covid-19 của Việt Nam do Học viện Quân y và Công ty CP công nghệ Việt Á phối hợp nghiên cứu và sản xuất.
Theo đó, WHO đã đánh giá bộ kit LightPower iVA SARS-CoV-2 1st RT-rPCR Kit do Công ty Việt Á sản xuất, theo Quy trình Danh sách Sử dụng Khẩn cấp (EUL) và cấp mã số EUL 0524-210-00.
Trước đó, Bộ Y tế và Chăm sóc xã hội Anh cũng đã cấp giấy chứng nhận đạt tiêu chuẩn châu Âu (CE) và cấp giấy chứng nhận lưu hành tự do (CFS) cho bộ sản phẩm xét nghiệm Covid-19 LightPower iVA SARS-CoV-2 1st RT-rPCR nêu trên. Cơ quan Quản lý thuốc và các sản phẩm chăm sóc sức khỏe Anh (MHRA) đã gửi chứng nhận cho Công ty cổ phần Công nghệ Việt Á
MHRA đã tiến hành kiểm định chất lượng, thử nghiệm trong thực tế và cấp phép cho bộ sản phẩm trên.
Bộ kít xét nghiệm iVA SARS-CoV-2 1st RT-rPCR, được Bộ Khoa học Công nghệ Việt Nam giao Học viện Quân y và Công ty Việt Á phối hợp nghiên cứu, sản xuất. Bộ kít xét nghiệm này đã được sử dụng tại Việt Nam với hiệu quả phát hiện bệnh tốt. Rất nhiều quốc gia trên thế giới đã đặt hàng Việt Nam sản xuất bộ kít xét nghiệm SARS-CoV-2 này.
Với chứng nhận này, bộ kít xét nghiệm Covid-19 của Việt Nam có thể được bán tự do ở tất cả các quốc gia thành viên của Khu vực kinh tế châu Âu bao gồm Vương quốc Anh.
Sau khi được Bộ Y tế và Chăm sóc xã hội Anh cấp phép, bộ kít xét nghiệm Covid-19 của Việt Nam đã được một đối tác đặt mua để phân phối tại Anh, Ấn Độ, Mexico, Mỹ và một số quốc gia tại châu Âu với số lượng cam kết ít nhất 1 triệu test/tháng. Việc có thêm sự chấp thuận của WHO sẽ giúp sản phẩm dễ dàng được xuất khẩu ra các nước trên toàn thế giới.
Mời các bạn đồng hành cùng báo Dân Việt trên mạng xã hội Facebook để nhanh chóng cập nhật những tin tức mới và chính xác nhất.
Tin cùng chuyên mục
Xem theo ngày
Xem
Tin nổi bật








Vui lòng nhập nội dung bình luận.