- Bầu cử Tổng thống Mỹ 2024
- Nhìn lại Hội nghị Thủ tướng đối thoại với nông dân 2023
- Chủ tịch Hội NDVN- Bộ trưởng TNMT lắng nghe nông dân nói
- Kỷ nguyên mới - Kỷ nguyên vươn mình
- Tháo gỡ điểm nghẽn thể chế
- Kỳ họp thứ 8 Quốc hội khóa XV
- Căng thẳng Triều Tiên - Hàn Quốc đang gia tăng
- Diễn đàn Nông dân quốc gia lần thứ IX - 2024
Chủ đề nóng
- Đăng nhập
- Đăng ký
- ×
Vui lòng đăng nhập hoặc đăng ký để gửi bình luận
Khi nhấn đăng nhập đồng nghĩa với việc bạn đã đồng ý với điều khoản sử dụng của báo Dân Việt
Đăng nhập
Họ và tên
Mật khẩu
Mã xác nhận

Khi nhấn đăng ký đồng nghĩa với việc bạn đã đồng ý với
điều khoản sử dụng của
báo Dân Việt
Đăng ký
Xin chào, !
Bạn đã đăng nhập với email:
Đăng xuất
Vắc xin Covid-19 thứ 2 của Việt Nam chuẩn bị thử nghiệm lâm sàng
Diệu Linh
Thứ bảy, ngày 27/02/2021 10:54 AM (GMT+7)
Sáng 27/2, ông Dương Hữu Thái - Giám đốc Viện Vắc xin và sinh phẩm y tế Nha Trang (IVAC) cho biết, vắc xin Covid-19 COVIVAC do công ty sản xuất sẽ có giá không quá 60.000 đồng/liều, đáp ứng nhu cầu của người dân Việt Nam.
Bình luận
0
Sáng 27/2, tại Bộ Y tế, đã diễn ra Lễ tiếp nhận 20 tỷ đồng để nghiên cứu thử nghiệm lâm sàng vắc xin phòng ngừa Covid-19 “Made in Vietnam” COVIVAC do Tập đoàn Vingroup tài trợ cho Viện Vắc xin và Sinh phẩm Y tế (IVAC) trực thuộc Bộ Y tế sản xuất.
Trước Tết, tại trường Đại học Y Hà Nội đã tiến hành tuyển tình nguyện viên tham gia thử nghiệm vắc xin ngừa Covid-19 COVIVAC do IVAC sản xuất. Dự tính đầu tháng 3 sẽ tiêm liều vắc xin COVIVAC đầu tiên trên tình nguyện viên.
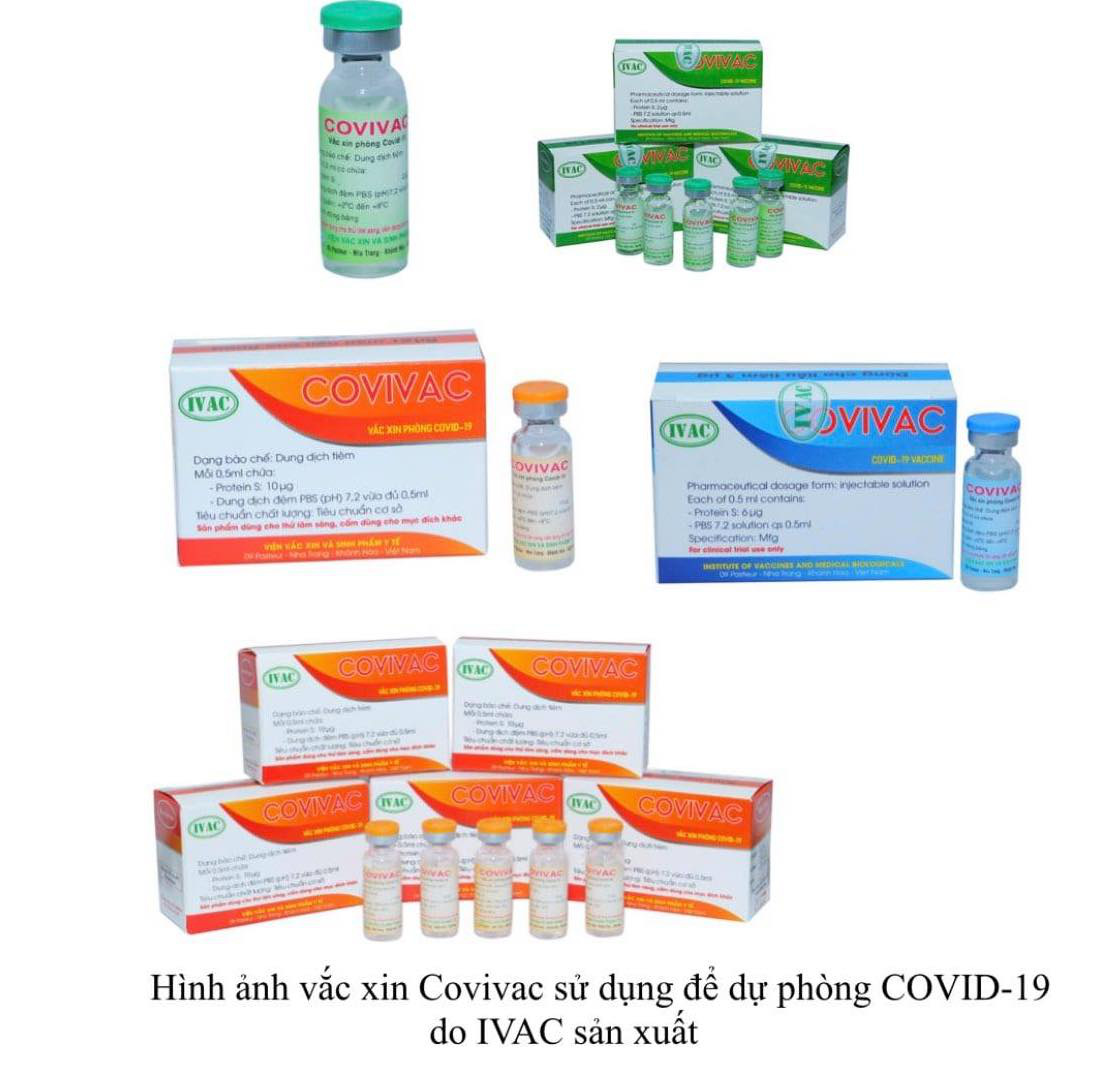
Vắc xin Covid-19 COVIVAC
Phát biểu tại buổi lễ, Bộ trưởng Bộ Y tế Nguyễn Thanh Long nhấn mạnh: “Nhân dịp hôm nay là ngày kỷ niệm 66 năm Ngày Thầy thuốc Việt Nam (27/2/1955 – 27/2/2021), tôi đánh giá sự kiện này là một hoạt động ý nghĩa giúp thúc đẩy nhanh quá trình thử nghiệm lâm sàng của loại vắc xin phòng ngừa Covid-19 “Made in Vietnam”. Từ đó, Việt Nam có thêm nhiều cơ hội đánh giá khoa học một cách đầy đủ, toàn diện để khẳng định tính khả thi của vắc xin COVIVAC đạt hiệu quả, có tính an toàn và hiệu quả.
Tôi tin tưởng rằng, ngành y tế sẽ đạt được kết quả tốt trong nghiên cứu vắc xin phòng ngừa Covid-19 tiến tới Việt Nam sớm hoàn toàn tự chủ nguồn vắc xin này".
"Thời gian qua các nhà khoa học Việt Nam coi việc sản xuất vắc xin Covid-19 một cách rất cấp thiết. Chúng ta vừa đặt mua vắc xin Covid-19, vừa thúc đẩy sản xuất trong nước. Đó là vì sự biến chủng của virus SARS-CoV-2, hiệu lực bảo vệ vắc xin chỉ trong thời gian nhất định, chúng ta phải chủ động, coi vấn đề vắc xin là vấn đề an ninh sức khỏe
Sau vắc xin Covid-19 Nano Covax, COVIVAC sẽ được tiến hành thử nghiệm lâm sàng. Thời gian ngắn tới sẽ có vắc xin Covid-19 thứ 3 do Việt Nam sản xuất sẽ được tiến hành thử nghiệm.
Chúng ta tự tin thời gian tới sẽ chủ động được nguồn vắc xin Covid-19.
Tuy nhiên mọi bước đi phải thận trọng để đảm bảo cung cấp cho người dân vắc xin đảm bảo an toàn, hiệu quả nhất".
Bộ trưởng Bộ Y tế Nguyễn Thanh Long
Xuất phát từ tình hình nghiên cứu vắc xin tại Việt Nam, nhằm chung tay phòng chống dịch bệnh, bảo vệ sức khỏe người dân, tập đoàn Vingroup đã quyết định trao tặng Viện Vắc xin và Sinh phẩm Y tế kinh phí là 20 tỷ đồng để tài trợ cho hoạt động nghiên cứu thử nghiệm lâm sàng Vắc xin COVIVAC.
Công nghệ sản xuất vắc xin Covid-19 đã dùng để sản xuất vắc xin cúm thành công
Dự án nghiên cứu thử nghiệm vắc xin COVIVAC của Viện Vắc xin và Sinh phẩm Y tế (IVAC) trực thuộc Bộ Y tế được nghiên cứu từ tháng 5/2020, trên cơ sở hợp tác với các Trường đại học, Viện nghiên cứu và các Tổ chức quốc tế sản xuất.
Theo ông Dương Hữu Thái, COVIVAC là vắc xin dạng dung dịch có hoặc không có tá chất bổ trợ, không có chất bảo quản, với công nghệ sản xuất là vắc xin vector Newcastle (NDV), gắn gen biểu hiện Protein S của virus SARS-CoV-2 dựa trên công nghệ sản xuất trên trứng gà có phôi. Công nghệ này cũng được sử dụng để sản xuất vắc xin dự phòng cúm mùa đang lưu hành tại Việt Nam.

Nhiều bạn trẻ đã đến tham gia đăng ký làm tình nguyện viên thử nghiệm vắc xin Covid-19 COVIVAC
Kết quả thực hiện các nghiên cứu tiền lâm sàng tại Ấn Độ, Mỹ và Việt Nam đến thời điểm này đã cho thấy tính an toàn và hiệu quả trên thực nghiệm. Sau 7 tháng nghiên cứu tháng (5/2020-12/2020), IVAC đã sản xuất thành công 3 lô liên tiếp trên quy mô lớn từ 50 ngàn đến 100 ngàn liều mỗi lô.
Các lô vắc xin dự tuyển thử nghiệm lâm sàng đã được đánh giá chất lượng tại nhà sản xuất và Viện Kiểm định quốc gia NICVB, NICVB đã cấp giấy chứng nhận đạt yêu cầu chất lượng 6 lô vắc xin thành phẩm. Vắc xin COVIVAC cũng đã thử Tiền lâm sàng về độc tính, đáp ứng miễn dịch, hiệu quả bảo vệ trên động vật thí nghiệm ở trong nước và nước ngoài.
Đề cương nghiên cứu lâm sàng giai đoạn 1 và giai đoạn 2 của vắc xin COVIVAC đã được Hội đồng Đạo đức trong nghiên cứu y sinh học quốc gia và Hội đồng đạo đức cấp cơ sở của các đơn vị liên quan chấp thuận. Viện Vắc xin và Sinh phẩm Y tế dự kiến sẽ bắt đầu tiến hành thử nghiệm lâm sàng vào tháng 3/2021 và dự kiến hoàn thành vào tháng 10/2021.
"Tôi hy vọng, COVIVAC sẽ sớm được thử nghiệm thành công, cung cấp cho người Việt Nam một vắc xin chất lượng, giá thành rẻ. Chúng tôi dự kiến vắc xin Covid-19 COVIVAC sẽ có giá không quá 60.000 đồng/liều", ông Thái chia sẻ.
Thông tin về nghiên cứu thử nghiệm lâm sàng gồm 2 giai đoạn 1 và 2 của vắc xin Covid-19 COVIVAC
Đơn vị nhận thử nghiệm là Viện Vệ sinh dịch tễ Trung ương (NIHE) và Trường Đại học Y Hà Nội. Đơn vị nhận tài trợ là Viện Vắc-xin và Sinh phẩm Y tế (IVAC).
Giai đoạn 1: thực hiện tại trường Đại Học Y Hà Nội:
- Tình nguyện viên tham gia nghiên cứu 120 người khỏe mạnh, độ tuổi từ 18-59 tuổi, cả nam và nữ;
- Người tình nguyện tham gia nghiên cứu sẽ được tiêm 2 mũi/ 0,5 ml (tiêm vắc xin hoặc tiêm giả dược) cách nhau 28 ngày.
- Giai đoạn 1 sẽ nghiên cứu độ an toàn và tính sinh miễn dịch trên 4 nhóm vắc xin với các mức liều 1 mcg, 3 mcg, 10 mcg kháng nguyên Protein S không có tá chất và 1 mcg có tá chất, có thêm nhóm đối chứng là giả dược (không chứa thành phần phần vắc xin).
- Mục tiêu: đánh giá độ an toàn và khả năng đáp ứng miễn dịch để chọn ra 2 nhóm vắc xin tối ưu nhất, chuyển sang nghiên cứu ở giai đoạn 2.
- Sau tiêm mũi 1, các tình nguyện viên sẽ được theo dõi y tế trong vòng 24h tại Trung tâm Dược lý lâm sàng, Đại Học Y Hà Nội.
- Sau tiêm mũi 2, thời gian theo dõi y tế các tình nguyện viên là 4 giờ.
Giai đoạn 2: thực hiện tại Trung tâm y tế Huyện Vũ Thư, tỉnh Thái Bình:
- Tình nguyện viêm tham gia nghiên cứu 300 người, khỏe mạnh, độ tuổi từ 18-75 tuổi (trong đó tuổi từ 60-75 chiếm khoảng 1/3), cả nam và nữ.
- Sau giai đoạn 1: sau 43 ngày nếu kết quả an toàn miễn dịch tốt, chọn được mức liều tối ưu sẽ tiếp nối chuyển sang nghiên cứu giai đoạn 2.
- Người tình nguyện tham gia nghiên cứu sẽ được tiêm 2 mũi/ 0,5 ml (tiêm vắc xin hoặc tiêm giả dược) cách nhau 28 ngày.
- Giai đoạn 2 sẽ nghiên cứu độ an toàn và tính sinh miễn dịch trên 2 nhóm vắc xin với các mức liều tối ưu chọn dược từ giai đoạn 1, có thêm nhóm đối chứng là giả dược (không chứa thành phần phần vắc xin).
- Mục tiêu: phối hợp dự liệu với giai đoạn 1 để đánh giá độ an toàn và hiệu lực đáp ứng miễn dịch của 2 nhóm vắc xin ở quần thể lớn hơn, xem xét chuyển sang nghiên cứu ở giai đoạn 3.
- Thời gian lưu lại sau tiêm mũi 1 và mũi 2 của các tình nguyện viên ở giai đoạn 2 là từ 30-60 phút.
Tin cùng chủ đề: Vắc xin Covid-19 của Việt Nam
- Khánh Hòa đề xuất thí điểm sử dụng vắc xin Nano Covax
- Phân bổ vắc xin Covid-19 đợt 2 cho 63 tỉnh thành, TP.HCM, Hà Nội được nhiều nhất
- Phó Thủ tướng Vũ Đức Đam: Việt Nam sẽ sử dụng tốt món quà vắc xin Covid-19 của COVAX
- Không có ca Covid-19 mới, tăng cường công tác tiêm vắc xin Covid-19
Mời các bạn đồng hành cùng báo Dân Việt trên mạng xã hội Facebook để nhanh chóng cập nhật những tin tức mới và chính xác nhất.
Tin cùng chuyên mục
Xem theo ngày
Xem
Tin nổi bật










Vui lòng nhập nội dung bình luận.